適用于成人患者大血管(如主動脈�����、股動脈和頸動 脈)的開放性手術(shù)修復(fù)���,可作為標(biāo)準(zhǔn)止血方法(如縫合線和縫合針)的輔助手段的外科用封合劑,在我國屬于第三類醫(yī)療器械注冊產(chǎn)品�。該產(chǎn)品由預(yù)填充注射器和配件組成。預(yù)填充注射器填充了 45%牛血清白蛋白溶液和10%戊二醛溶液����。配件由標(biāo)準(zhǔn)混合管、尖端涂抹器混合管���、尖端延長管混合管組成��。
引言:適用于成人患者大血管(如主動脈�����、股動脈和頸動
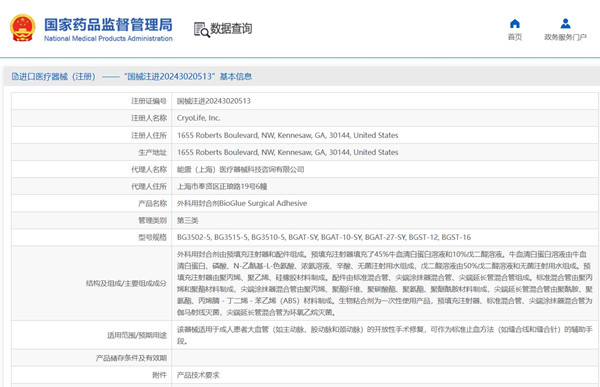
脈)的開放性手術(shù)修復(fù)�,可作為標(biāo)準(zhǔn)止血方法(如縫合線和縫合針)的輔助手段的外科用封合劑,在我國屬于第三類醫(yī)療器械注冊產(chǎn)品����。該產(chǎn)品由預(yù)填充注射器和配件組成。預(yù)填充注射器填充了 45%牛血清白蛋白溶液和10%戊二醛溶液���。配件由標(biāo)準(zhǔn)混合管�、尖端涂抹器混合管�����、尖端延長管混合管組成�����。產(chǎn)品為一次性使用�,預(yù)填充注射器、標(biāo)準(zhǔn)混合管��、尖端涂抹器混合管為伽馬射線滅菌��,尖端延長管混合管為環(huán)氧乙烷滅菌���。
一�、外科用封合劑注冊產(chǎn)品工作原理
外科用封合劑是一種雙組分的外科粘合劑,由純化的牛血清白蛋白(BSA)溶液和戊二醛構(gòu)成�����。采用雙腔針管��、標(biāo)準(zhǔn)混合管以及可選混合管構(gòu)成的輸送系統(tǒng)來涂抹溶液�。按預(yù)定比例配制的溶液在標(biāo)準(zhǔn)混合管內(nèi)混合,并發(fā)生交聯(lián)�����。戊二醛分子與牛血清白蛋白分子形成共價結(jié)合(交聯(lián))�,接觸修復(fù)部位的組織蛋白質(zhì)時���,將形成一個柔性的機械密封層��,這種作用不依賴于人體的凝血機制�����。輸送系統(tǒng)可使外科用封合劑的組分在體外反復(fù)混合����。外科用封合劑在20-30秒鐘內(nèi)開始進行聚合,在2分鐘內(nèi)達到其粘合強度��。外科用封合劑也能通過人工血管基質(zhì)的間隙形成機械式聯(lián)鎖�,粘合到人工血管的基質(zhì)之上。
二���、外科用封合劑產(chǎn)品技術(shù)要求
外科用封合劑產(chǎn)品性能評價初常規(guī)性能指標(biāo)外��,還應(yīng)包括:戊二醛
中甲醇濃度�、戊二醛分析集相關(guān)雜質(zhì)分析���、BSA與戊二醛交聯(lián)過程的吸/放熱性能��、聚合后BSA測定�、微生物指標(biāo)�����、聚合后戊二醛殘留等����。
三、外科用封合劑產(chǎn)品注冊要點
1.外科用封合劑注冊產(chǎn)品生物相容性要做哪幾項����?
外科用封合劑注冊產(chǎn)品為與組織和組織液接觸的持久植入器械�,依據(jù) GB/T16886系列標(biāo)準(zhǔn)對其進行了生物相容性評價��,進行了細胞毒�、
致敏反應(yīng)、皮內(nèi)反應(yīng)�、遺傳毒性、血液相容性��、植入����、亞慢
性毒性、急性全身毒性和熱原測試�����;對于配件也進行了細胞
毒性試驗���、致敏試驗、皮內(nèi)反應(yīng)試驗�����、溶血試驗及急性毒性試驗。
2.外科用封合劑注冊產(chǎn)品滅菌方式選擇
外科用封合劑注冊產(chǎn)品由預(yù)填充注射器和配件(包括標(biāo)準(zhǔn)混合管��、尖端涂抹器混合管����、尖端延長管混合管)組成,預(yù)填充注射器����、標(biāo)準(zhǔn)混合管、尖端涂抹器混合管為伽馬射線滅菌���,尖端延長管混合管為環(huán)氧乙烷滅菌����。申請人提供了滅菌確認報告����,證明滅菌后的無菌保證水平均可達到10-6。
3.外科用封合劑注冊產(chǎn)品有效期和包裝
申報產(chǎn)品包括預(yù)填充注射器和配件(包括標(biāo)準(zhǔn)混合管���、
尖端涂抹器混合管����、尖端延長管混合管),其中���,預(yù)填充注射器 BG3510-5的滅菌有效期為24個月�,預(yù)填充注射器
BG3502-5 為 21 個月�,預(yù)填充注射器 BG3515-5為18個月。配件的滅菌有效期為60個月�。申請人提供了加速老化的有效期驗證報告和實時有效期驗證報告,并按照化學(xué)藥品與包裝材料相容性研究指導(dǎo)原則開展了相容性驗證研究�。
如有外科用封合劑注冊或其他第三類醫(yī)療器械注冊咨詢服務(wù)需求,歡迎您隨時方便與杭州證標(biāo)客醫(yī)藥技術(shù)咨詢有限公司聯(lián)絡(luò)����,聯(lián)系人:葉工,電話:18058734169��,微信同����。